طراحی واکسنی جدید برای بیماری آلزایمر

پژوهشگران مرکز پزشکی دانشگاه تگزاس اخیرا گزارش کردند که آنها واکسنی را طراحی کردهاند که میتواند بدن را در حمله به پلاکهای آمیلوئیدی و کلافههای نوروفیبریلی بیماری آلزایمر قبل از اینکه مغز را مختل کنند، مسلح کند. آنها امیدوارند که این واکسن را بهزودی روی انسانها آزمایش کنند. واکسن جدید برای نخستین بار پلاکهای حاوی آمیلوئید و پروتئین تائو را که هر دو شاخصیهایی برای تشخیص قطعی بیماری آلزایمر هستند، مورد هدف قرار میدهد. در این واکسنها از DNAی پروتئینهای آلزایمر برای آموزش سیستم ایمنی در جهت مبارزه با این عناصر و جلوگیری از تجمع آنها در مغز استفاده میشود. پژوهشگران میگویند که این واکسن جدید آلزایمر که DNA Aβ42 نامیده میشود، میتواند تعداد موارد زوال عقل را به نصف برساند. پژوهشگران نتایج این مطالعه را در ژورنال Alzheimer’s & Research Therapy منتشر کردند.
واکسن جدید بر خلاف موارد پیشین، از طریق تزریق سطحی در پوست استعمال میشود. نمونههای قبلی که بهصورت تزریق عضلانی در موشها مورد استفاده قرار میگرفتند، موجب تورم مغز میشدند. پس از تزریق پوستی واکسن جدید، یک زنجیرهی سهملکولی (تریمر) از بتاآمیلوئید در پوست ساخته شده و بدن با تولید آنتیبادیهایی که مانع از افزایش آمیلوئید و تائو میشود، به این ملکولها پاسخ میدهد. راجر روزنبرگ نویسندهی مقاله میگوید:
اهمیت این یافتهها این است که ایمنیدرمانی تریمر DNA Aβ42 دو عامل بیماریزای بیماری آلزایمر یعنی پلاکهای آمیلوئید و کلافههای نوروفیبریل را بدون ایجاد پاسخ التهابی سلولهای T که خطر بروز التهاب خودایمنی را به همراه دارند، مورد هدف قرار میدهد.
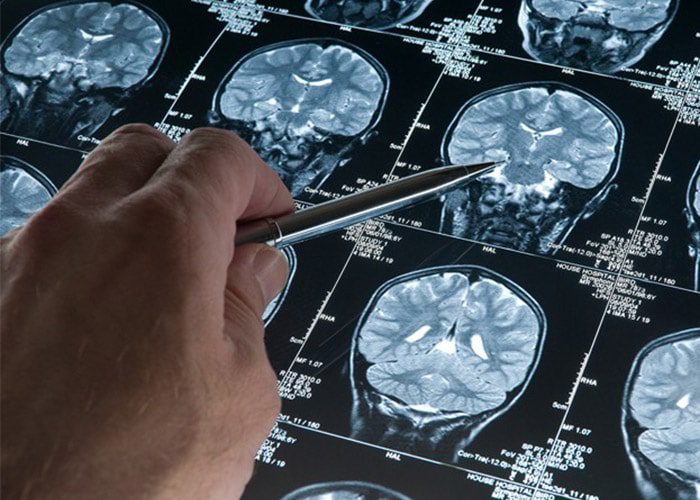
از آنجایی که در حال حاضر پژوهشگران بهطور دقیق نمیدانند که چه زمانی تجمع آمیلوئید و تائو آغاز میشود، روزنبرگ میگوید که پزشکان با انجام اسکنهای مغزی میتوانند تعیین کنند که چه زمانی این واکسن باید استفاده شود.
اگرچه پژوهش روزنبرگ ارتباطی با مطالعه رادولف تانزی، دانشمند دانشگاه هاروارد که ژنهای مرتبط با آغاز آلزایمر را مورد مطالعه قرار داد، ندارد ولی هر دو به یک موضوع اشاره دارند: با کم نگهداشتن سطح آمیلوئید، از بروز آلزایمر اجتناب کنید.
آزمایشگاه تانزی در بیمارستان عمومی ماساچوست در حال مکانیابی میکروبیوم مغز است؛ جمعیتی از میکروارگانیسمها که برخی مفید بوده و برخی بیماریزا هستند و درون مغز وجود دارند. پژوهشگران در پروژه میکروبیوم مغز، بهدنبال یافتن شایعترین میکروبها در مغز هستند. هدف آنها این است که تعیین کنند کدام میکروبها میتوانند منجر به بروز بیماری آلزایمر شوند. با استفاده از این اطلاعات، آنها امیدوارند که درمانهایی برای پیشگیری و درمان این بیماری پیدا کنند.
این کار جدای سیستم کشت سهبعدی سلولهای عصبی یا مدل بیماری آلزایمر در یک ظرف (ارگانوئیدهای شبیهسازیشده از مغز انسان) است که تانزی و دکتر دو توئن کیم با استفاده از ژنهای آلزایمر ایجاد کردند. این سیستم اساسا وضعیتی تقلیدی از فرایندهای تشکیل پلاکها و کلافهها در بیماری آلزایمر است. با استفاده از این سیستم، تانزی دارویی برای بیماری آلزایمر معرفی کرد که حاوی تنظیمکنندههای آنزیم گاما سکرتاز و چاپرونهای فلزی برای کم کردن بتا آمیلوئید و تشکیل کلافههای نوروفیبریلی در مغز بود.
او گفت این پژوهش فوقالعاده پیچیده است؛ دانشمندان از سلولهای بنیادی برای تولید سلولهای عصبی انسان استفاده کردند. سپس آنها را در ژلی قرار دادند تا مغز انسان را شبیهسازی کنند و توانستند کل فرایند بیماریزایی آلزایمر را در ظروف آزمایشگاهی ایجاد کنند. این کار به آنها این امکان را میداد که بتوانند حوادث واقعی را که بهطور معمول طی چند دهه پیش میآید، مشاهده کنند: تشکیل پلاکهای آمیلوئید که سپس منجر به تشکیل کلافهها و التهاب در مغز میشوند.
تانزی گفت مدل آلزایمر در یک ظرف مسئلهای بهقدمت چند دهه را در مورد اینکه آیا پلاکهای آمیلوئید یا کلافههای نوروفیبیرلی برای بیماری آلزایمر باید مورد سرزنش قرار گیرند، حل کرد. دیگر تردیدی وجود ندارد؛ تمام دادهها میگویند که اگر شما مقدار آمیلوئید را کم نگه دارید، آلزایمر را متوقف خواهید کرد. او میگوید:
ما تا زمانی که علایم آلزایمر قابل مشاهده شوند، آن را مورد درمان قرار نمیدهیم و در این زمان علت آن یعنی پلاکهای آمیلوئیدی را درمان میکنیم. لازم است که تشکیل پلاکهای آمیلوئیدی را ۱۰ تا ۲۰ سال قبلتر از آنکه علایم در فرد قابل مشاهده شوند، متوقف کنیم. ما اکنون میتوانیم با استفاده از تصویربرداری از مغز و بیومارکرهایی، احتمال اینکه یک فرد در مراحل بعدی زندگی دچار آلزایمر شود را تعیین کنیم؛ درست مانند کاری که پزشکان با آزمایش کلسترول برای بیماری قلبی انجام میدهند. در آینده نزدیک، تستهای خونی برای آلزایمر نیز وجود خواهد داشت.
تانزی امیدوار است که در آیندهای نزدیک، بههمین ترتیب که آمریکاییها از دارویی برای پیشگیری از تجمع کلسترول استفاده میکنند، دارویی نیز برای پایین نگهداشتن سطوح آمیلوئید مغز ارائه شود.
روش دیگر هم استفاده از واکسن روزنبرگ خواهد بود. پژوهشگران در مطالعه خود نوشتند:
ما برای اولین بار با مطالعه روی یک موشهای مبتلا به آلزایمر گزارش میکنیم که ایمنیدرمانی با استفاد از DNA Aβ42 فعال در پوست دو عامل بیماریزا را مورد هدف قرار میدهد: پلاکهای حاوی آمیلوئید و تائو.
واکسیناسیون DNA که در آن آنتیژنی (پپتید یا پروتئین) موجود نیست اما DNAی کدکننده این پپتید وجود دارد، روش دیگری برای واکسیناسیون است. ژنهای کدشده توسط DNA در پوست بیان پیدا میکنند و این پپتیدها توسط سلولهای دندریتیک به گرههای لنفی محلی برده شده و با سلولهای T و B مواجه میشوند.
پژوهشگران مرکز پزشکی دانشگاه تگزاس نشان دادهاند که ایمنیدرمانی تریمر DNA Aβ42 فرایندی غیرالتهابی بوده و موجب پاسخ ایمنی میشود که در حذف آمیلوئید از مغز موشهای ترانسژنیک موثر است. اکنون آنها دریافتهاند که ایمنیدرمانی با تریمر DNA Aβ42 منجر به کاهش پپتیدهای آمیلوئید و پلاکهای آمیلوئید میشود. برای نخستین بار است که ایمنیدرمانی DNA Aβ42 منجر به کاهش قابلتوجهی در پروتئين تائو در معز موش میشود.
آلزایمر بهعنوان یک بیماری تخریبکنندهی عصب، شایعترین فرم زوال عقل است که در جمعیت مسن مشاهده میشود. روزنبرگ و دانشمندان دیگر برای سالها معتقد بودهاند که ایمنیدرمانی با هدف مبارزه با تجمع آمیلوئید در مغز میتواند درمان ممکنی برای آلزایمر باشد و ممکن است بتواند به جلوگیری از پیشرفت بیماری کمک کند. تعدادی از روشهای ایمنیدرمانی که قبلا انجام شده بودند، بینتیجه بودهاند. یکی از این موارد، روشی بود که پژوهشگران متوجه شدند موجب بروز بیماری انسفالیت خودایمنی در ۶ درصد از بیماران میشود.
امروزه بیماری آلزایمر ششمین علت مرگومیر در آمریکا است. این بیماری مغز افراد مبتلا را دچار مشکل میکند؛ پروتئینهای آمیلوئید بتا، با افزایش سن در مغز به هم میچسبند و کلافههایی از پروتئینهای تائو تشکیل میشود که مانع از ارتباطات عصبی میشوند. درمانی برای این بیماری وجود ندارد و در حال حاضر فقط گزینههای درمانی در جهت کاهش علایم در دسترس هستند. ویژگیهای پاتوژنیک پلاکهای آمیلوئیدی و کلافههای نوروفیبریلی علایم تشخیص قطعی بیماری آلزایمر محسوب میشوند و منشا و توسعهی بیماری بهطور قوی با تجمع آمیلوئید بتا در مغز مرتبط بوده است. حدود ۳۰ سال پیش، فرضیه آبشار آمیلوئید با این فرض که رسوب آمیلوئید اولین رویداد منجر به بیماری آلزایمر است، ارائه شد.
واکسن روزنبرگ که در پوست اعمال میشود، موجب تولید یک زنجیرهی سه ملکولی از بتاآمیلوئید در سلولهای پوست میشود. در این وضعیت سیستم ایمنی فعال میشود تا آنتیبادیهایی برای مبارزه با پروتئین تائو و آمیلوئید بتا تولید کند. پژوهشگران این واکسن را روی چهار گروه از موشها آزمایش کردهاند. کاهش ۴۰ درصدی در پلاکهای آمیلوئیدی در موشهای واکسینهشده مشاهده شد و تا ۵۰ درصد از میزان کلافههای تائو نیز در مغزشان کم شد.
پژوهشگران گفتهاند که آنها پاسخ ایمنی نامطلوبی در ارتباط با این واکسن مشاهده نکردند و این نتایج نشان میدهد که با این واکسن، بدن برای حمله به پلاکهای آمیلوئید و کلافههای تائو قبل از اینکه اینها شروع به از کار انداختن مغز کنند، مسلح میشود.